
Kali (tên Latinh: Kalium) là yếu tố hoá học tập ký hiệu K, số trật tự 19 vô bảng tuần trả. Kali yếu tố là sắt kẽm kim loại kiềm mượt, đem white color bạc, dễ dẫn đến ôxy hóa nhanh chóng vô không gian và phản xạ cực mạnh với nước đưa đến một lượng sức nóng đầy đủ nhằm châm cháy lượng hyđrô sinh rời khỏi vô phản xạ này. Kali cháy đem ngọn lửa được màu tím hoa cà.
Bạn đang xem: Kali (K)

Màu của ngọn lửa khi châm kali hoặc những ăn ý hóa học của kali.
Lịch sử hình thành:
Không nên những muối hạt kali hoặc natri từng được nghe biết vô thời kỳ La Mã, và tên thường gọi Latin của yếu tố này sẽ không nên gốc Latin truyền thống nhưng mà là Tân Latin. Tên Latin kalium được lựa chọn kể từ từ “alkali” và đã được gửi tự động kể từ tiếng Ả Rập: القَلْيَه al-qalyah tức là “tro thực vật”. Thuật ngữ alkali trị âm tượng tự động vô giờ Anh cũng có thể có nằm trong gốc này (potassium vô giờ Ả Rập chuẩn chỉnh văn minh là بوتاسيوم būtāsyūm).
Tên giờ Anh của yếu tố này là potassium bắt mối cung cấp kể từ từ “potash”, nói đến một cách thức nhưng mà Từ đó potash nhận được bằng phương pháp thanh lọc tinh khiết tro mộc hoặc lá cây và thực hiện cất cánh khá hỗn hợp vô một chiếc nồi. Potash về thực chất là 1 trong lếu láo ăn ý muối hạt kali bởi thực vật đem có một không nhiều hoặc không tồn tại dung lượng natri, và phần sót lại của khoáng hóa học vô thực vật bao hàm những muối hạt can xi đem tính hòa tan kha khá thấp. Trong khi kali từng được dùng kể từ thời kỳ thượng cổ, tuy nhiên nó ko được nghe biết vô xuyên suốt bề dày lịch sử hào hùng là 1 trong hóa học khác lạ về cơ bạn dạng với những muối hạt natri. Georg Ernst Stahl vẫn nhận được vày xác nhận nghiệm được chấp nhận ông tóm lại sự khác lạ của những ham muốn natri và kali vô năm 1702, và Henri Louis Duhamel du Monceau vẫn hoàn toàn có thể minh chứng sự khác lạ này vô năm 1736. Thành phần chất hóa học đúng mực của những ăn ý hóa học natri và kali, và tình trạng yếu tố natri và kali đang không được nghe biết, và bởi vậy Antoine Lavoisier đang không xếp alkali vô vào list những yếu tố chất hóa học của ông năm 1789.
Kim loại kali và đã được Sir Humphry Davy trị hiện nay năm 1807, ông tách nó rời khỏi kể từ người yêu ghé ăn domain authority (KOH). Kim loại kiềm này là sắt kẽm kim loại trước tiên được pha chế vày năng lượng điện phân muối hạt giá chảy với cùng 1 voltaic pile được trị hiện nay tiên tiến nhất. Kali là sắt kẽm kim loại trước tiên được pha chế vày cách thức năng lượng điện phân. Cùng năm bại liệt, Davy vẫn thông tin về sự việc tách natri sắt kẽm kim loại từ là một dẫn suất khoáng chất (caustic soda, NaOH, hoặc lye) chứ không cần nên muối hạt thực vật cũng vày chuyên môn tương tự động, và ông vẫn minh họa rằng những yếu tố tách rời khỏi kể từ những muối hạt này là không giống nhau. Mặc cho dù việc phát triển sắt kẽm kim loại kali và natri vẫn đã cho chúng ta biết rằng bọn chúng là những yếu tố tuy nhiên nên mất mặt một khoảng tầm thời hạn trước lúc lời khuyên này được thừa nhận thoáng rộng.
Trong một thời hạn nhiều năm những phần mềm potash chỉ sử dụng trong những việc phát triển thủy tinh nghịch, dung dịch tẩy và xà chống. Xà chống kali kể từ mỡ động vật hoang dã và dầu thực vật có mức giá đặc biệt cao, bởi bọn chúng đem khuynh phía hòa tan nhiều hơn thế nội địa và mượt rộng lớn, nên gọi là xà chống mượt. Phát hiện nay của Justus Liebig năm 1840 đã cho chúng ta biết rằng kali là yếu tố quan trọng cho tới thực vật và đa số loại khu đất đều thiếu thốn kali đã trải ngày càng tăng nhu yếu những muối hạt kali. Tro mộc kể từ những loại cây linh sam lúc đầu được dùng như 1 mối cung cấp hỗ trợ muối hạt kali ở dạng phân bón, tuy vậy với việc trị hiện nay năm 1868 về những mỏ chứa chấp kali clorua sát Staßfurt, Đức thì sản lượng phân bón kali chính thức được phát triển ở quy tế bào công nghiệp. Các mỏ potash không giống dần dần được trị hiện nay, và vô những năm 1960 Canada phát triển thành nước phát triển mối cung cấp kali chủ yếu bên trên thị ngôi trường quốc tế.
Tính hóa học lý, hóa:
Kali đem những đặc thù của một sắt kẽm kim loại kiềm: mượt (cắt được vày dao), đem sức nóng nhiệt độ chảy và sức nóng phỏng sôi thấp, có tính dẫn năng lượng điện cao.
Kali đem đặc thù chất hóa học tương tự động natri. Kali sắt kẽm kim loại đem white color bạc, ánh kim, tuy nhiên khi xúc tiếp với không gian có khả năng sẽ bị gửi tức thì trở thành color xám đen ngòm, bại liệt là vì Kali sắt kẽm kim loại bị phủ một tờ KO2 ở ngoài nằm trong và bên phía trong là lớp K2O. Khi xúc tiếp với không gian độ ẩm, 2 lớp oxit này sẽ ứng dụng với khá nước tạo nên hidroxit rồi hidroxit kết phù hợp với khí cacbonic trở thành muối hạt cacbonat.

Sự thay cho thay đổi về sắc tố bên phía ngoài của Kali sắt kẽm kim loại (khi nhằm ngoài không gian và khi mới mẻ cắt)
Cũng tương tự Natri, Kali ứng dụng với hidro tạo nên hidrua ở 350-400oC, còn khi châm vô không gian hoặc vô oxi, Kali ngoài phản xạ với oxi tạo nên oxit, peoxit như Natri, còn tạo nên supeoxit KO2.
Khi cho tới tương tác với nước, Kali phản xạ mạnh mẽ rộng lớn Liti và Natri, bốc cháy ngay lúc gặp gỡ nước. Do bại liệt cần thiết cẩn trọng khi thực hiện thực nghiệm với Kali.
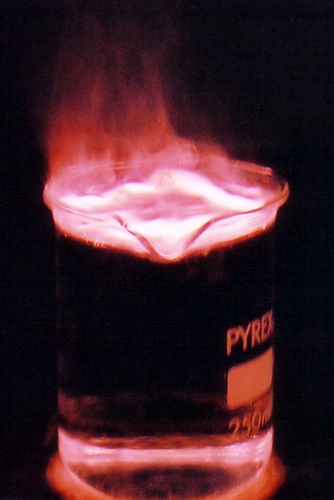
Kali bốc cháy khi gặp gỡ nước.
Kali ko ứng dụng thẳng với nitơ, cacbon, silic trong cả khi đun giá.
Đồng vị của Kali:
Có 24 đồng vị của kali và đã được biết, vô bại liệt đem 3 đồng vị đem vô tự động nhiên: K39 (93,3%), K40 (0,01%) và K41 (6,7%). Đồng vị đương nhiên K40 đem chu kỳ luân hồi cung cấp tung 1,250×109 năm và phân tung trở thành Ar40 (11,2%) bằng phương pháp bắt năng lượng điện tử và vày phản xạ positron, na ná phân tung trở thành đồng vị ổn định quyết định Ca40 (88,8%) vày phản xạ beta.
Sự phân tung của K40 trở thành Ar40 thường thì được dùng thực hiện cách thức nhận xét tuổi hạc những loại đá. Phương pháp nhận xét tuổi hạc vày tỷ trọng K/Ar tùy thuộc vào fake thiết rằng những loại đá ko chứa chấp agon ở thời khắc đưa đến nó và từng agon bởi phóng xạ sinh rời khỏi tiếp sau đó (Ar40) về mặt mày lượng là được bảo toàn, tức là 1 trong khối hệ thống kín. Các khoáng hóa học được xác lập tuổi hạc bằng phương pháp đo tỷ lệ của kali na ná lượng Ar40 bởi phóng xạ sinh rời khỏi và đã được thu thập. Các khoáng hóa học thích hợp nhằm xác lập tuổi hạc là biôtit, muscôvit, và plutonit/hocblen đổi mới hóa học, na ná fenspat núi lửa; toàn cỗ những khuôn đá kể từ nham thạch núi lửa và đá đột nhập nông hoàn toàn có thể được xác lập tuổi hạc nếu như bọn chúng khồng hề bị thay cho thế. Dường như, những đồng vị kali còn được dùng như thể hóa học lưu lại vết vô nghiên cứu và phân tích không khí. Chúng cũng khá được dùng trong số nghiên cứu và phân tích về quy trình vận gửi những dưỡng chất vì thế kali là dưỡng chất nhiều lượng quan trọng cho việc sinh sống.
K40 đem vô kali đương nhiên (và vì vậy đem trong số thành phầm muối hạt thương mại) vô một lượng vừa vặn đầy đủ đến mức độ một túi rộng lớn của những hóa học này hoàn toàn có thể dùng như mối cung cấp phóng xạ cho những minh họa vô lớp học tập. Tại người và động vật hoang dã khỏe khoắn, 40K là 1 trong mối cung cấp phóng xạ lớn số 1 thậm chí còn còn hơn hết 14C. Trong khung hình một người nặng nề 70 kg có tầm khoảng 4.400 phân tử nhân 40K phân tung từng giây. Mức phỏng phân tung của kali đương nhiên là 31 Bq/g.
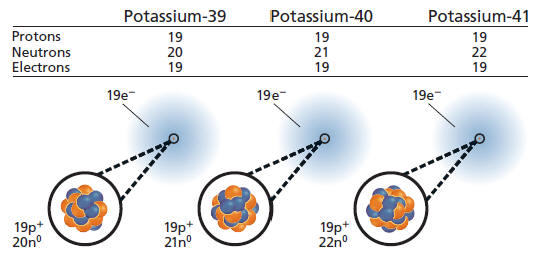
Ba đồng vị đem vô đương nhiên của Kali.
Phương pháp pha chế Kali:
Có thể pha chế Kali tương tự động như pha chế Natri.
Ứng dụng của Kali: Kali có rất nhiều phần mềm cần thiết vô nông nghiệp, đồ ăn thức uống, công nghiệp và những nghành nghề dịch vụ không giống.
- Trong nông nghiệp: người tớ sử dụng kali nhằm sản xuất những loại phân bón. Kali đem tầm quan trọng đa phần trong những việc gửi hoá tích điện vô quy trình đồng hoá những dưỡng chất của cây trái. Kali thực hiện tăng năng lực chống Chịu của cây trái so với những tác dụng ko lợi kể từ bên phía ngoài và chống Chịu so với một vài loại bệnh…
- Trong thực phẩm: chính sách ăn nhiều kali hoàn toàn có thể thực hiện tách nguy cơ tiềm ẩn tăng áp suất máu và đột quỵ.
- Trong công nghiệp: những ăn ý hóa học của kali đem tầm quan trọng cần thiết và thoáng rộng trong số ngành phát triển, như KOH vô phát triển muối hạt kali hoặc xà phòng; KNO3 sử dụng vô sản xuất dung dịch súng; KCN vô khai quật vàng, bạc,…; K2CrO4 dùng để làm sản xuất phẩm color, nhuộm,….
- Supeoxit KO2 là hóa học rắn color cam là mối cung cấp hỗ trợ ôxy tiện lợi và là hóa học hít vào cacbon dioxit. Nó được dùng thoáng rộng vô khối hệ thống thông khí mỏ, những tàu lặn và tàu không khí bởi nó chứa chấp không nhiều thể tích rộng lớn ôxy khí.
- Kali cobaltinitrit K3[Co(NO2)6] được sử dụng thực hiện hóa học tạo nên color của những họa sỹ với tên thường gọi Aureolin hoặc Coban vàng.
- Hợp kim của natri và kali, NaK ở dạng hóa học lỏng được sử dụng thực hiện hóa học trung gian giảo truyền sức nóng và thực hiện hóa học mút hút độ ẩm sẽ tạo rời khỏi một môi trường xung quanh không gian thô. Nó hoàn toàn có thể được dùng vô phản xạ chưng đựng.

Một loại phân bón đem chứa chấp Kali

Thực phẩm nhiều Kali
Bảng một vài đại lượng của Kali:
|
Tính hóa học chung |
|||||||||||||||||||||||||||||||
| Tên, Ký hiệu, Số | Kali, K, 19 | ||||||||||||||||||||||||||||||
| Phiên âm | /pɵˈtæsiəm/ po-TAS-ee-əm | ||||||||||||||||||||||||||||||
| Phân loại | Kim loại kiềm | ||||||||||||||||||||||||||||||
| Nhóm, Chu kỳ, Phân lớp | 1, 4, s | ||||||||||||||||||||||||||||||
| Khối lượng nguyên vẹn tử | 39,0983(1) | ||||||||||||||||||||||||||||||
| Cấu hình electron | [Ar] 4s1 | ||||||||||||||||||||||||||||||
| Số electron bên trên vỏ năng lượng điện tử | 2, 8, 8, 1 | ||||||||||||||||||||||||||||||
|
Tính hóa học vật lý |
|||||||||||||||||||||||||||||||
| Màu | Ánh kim White bạc | ||||||||||||||||||||||||||||||
| Trạng thái vật chất | Chất rắn | ||||||||||||||||||||||||||||||
| Mật phỏng sát sức nóng phỏng phòng | 0,862 g·cm−3 | ||||||||||||||||||||||||||||||
| Mật phỏng ở thể lỏng khi đạt sức nóng nhiệt độ chảy | 0,828 g·cm−3 | ||||||||||||||||||||||||||||||
| Nhiệt nhiệt độ chảy | 336,53 K, 63,38 °C, 146,08 °F | ||||||||||||||||||||||||||||||
| Nhiệt phỏng sôi | 1032 K, 759 °C, 1398 °F | ||||||||||||||||||||||||||||||
| Điểm tía trạng thái | 336.35 K (63°C), kPa | ||||||||||||||||||||||||||||||
| Nhiệt lượng giá chảy | 2.33 kJ·mol−1 | ||||||||||||||||||||||||||||||
| Nhiệt lượng cất cánh hơi | 76,9 kJ·mol−1 | ||||||||||||||||||||||||||||||
| Nhiệt dung | 29,6 J·mol−1·K−1 | ||||||||||||||||||||||||||||||
|
Tính hóa học nguyên vẹn tử Xem thêm: Cách tải Mega Huyền Thoại APK trên Android, iOS, PC đơn giản |
|||||||||||||||||||||||||||||||
| Trạng thái ôxi hóa | 1 (Bazơ mạnh) |
||||||||||||||||||||||||||||||
| Độ âm điện | 0,82 (thang Pauling) | ||||||||||||||||||||||||||||||
| Năng lượng ion hóa (thêm) |
Thứ 1: 418,8 kJ·mol−1 | ||||||||||||||||||||||||||||||
| Thứ 2: 3052 kJ·mol−1 | |||||||||||||||||||||||||||||||
| Thứ 3: 4420 kJ·mol−1 | |||||||||||||||||||||||||||||||
| Bán kính nằm trong hoá trị | 227 pm | ||||||||||||||||||||||||||||||
| Độ nhiều năm link nằm trong hóa trị | 203±12 pm | ||||||||||||||||||||||||||||||
| Bán kính nài der Waals | 275 pm | ||||||||||||||||||||||||||||||
| Thông tin cậy khác | |||||||||||||||||||||||||||||||
| Cấu trúc tinh nghịch thể | Lập phương tâm khối | ||||||||||||||||||||||||||||||
| Trạng thái trật tự động từ | Thuận từ | ||||||||||||||||||||||||||||||
| Điện trở suất | (20 °C) 72 nΩ·m | ||||||||||||||||||||||||||||||
| Độ dẫn nhiệt | 102,5 W·m−1·K−1 | ||||||||||||||||||||||||||||||
| Độ giãn nở nhiệt | (25 °C) 83,3 µm·m−1·K−1 | ||||||||||||||||||||||||||||||
| Tốc phỏng truyền tiếng động (thanh mỏng) | (20 °C) 2000 m·s−1 | ||||||||||||||||||||||||||||||
| Mô đun Young | 3,53 GPa | ||||||||||||||||||||||||||||||
| Mô đun cắt | 1,3 GPa | ||||||||||||||||||||||||||||||
| Mô đun nén | 3,1 GPa | ||||||||||||||||||||||||||||||
| Độ cứng bám theo thang Mohs | 0,4 | ||||||||||||||||||||||||||||||
| Độ cứng bám theo thang Brinell | 0,363 MPa | ||||||||||||||||||||||||||||||
| Số ĐK CAS | 7440-09-7 | ||||||||||||||||||||||||||||||
|
Chất đồng vị ổn định quyết định nhất |
|||||||||||||||||||||||||||||||
|
Bài chính: Đồng vị của Kali |
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
————————————————–
Bài viết lách đem dùng tư liệu kể từ những nguồn:
– Wikipedia (tiếng Việt và giờ Anh)
– SGK Hóa học tập 12 Nâng cao.
– Hoàng Nhâm (2005), Hóa học tập vô cơ, tập nhị, NXB Giáo Dục.
– Một số hình hình họa bên trên Google.
————————————————-
Xem thêm: Bí quyết đổi tên Facebook chỉ 1 chữ năm 2023, đặt tên FB 1 chữ trên Android và iPhone
Tham khảo thêm:
1. Vai trò của Kali so với cây trái.
2. Vai trò của Kali so với sức mạnh.











Bình luận