Để rất có thể học tập chất lượng môn Hóa thì việc ghi ghi nhớ bảng nhân tố hóa học là đòi hỏi yêu cầu. Đây cũng chính là kỹ năng cơ bạn dạng tiếp tục bám theo những em nhập xuyên suốt quy trình học tập cung cấp 2, cung cấp 3 và canh ty những em giải đúng mực những bài bác tập luyện tương quan. Sau đó là những kỹ năng về bảng nhân tố hóa học lớp 8 thông thường gặp gỡ và bài bác ca hóa trị dễ dàng học tập, dễ dàng ghi nhớ tuy nhiên Marathon Education ham muốn share cho tới những em.
>>> Xem thêm: Lý Thuyết Và Cách Học Thuộc Nhanh Bảng Tuần Hoàn Hóa Học Lớp 10
Bạn đang xem: Bảng hóa trị các nguyên tố hóa học | Marathon Education
Bảng hóa trị một trong những nhân tố chất hóa học thông thường gặp
|
Số proton |
Tên Nguyên tố |
Ký hiệu hoá học |
Nguyên tử khối |
Hoá trị |
|
1 |
Hiđro |
H |
1 |
I |
|
2 |
Heli |
He |
4 |
|
|
3 |
Liti |
Li |
7 |
I |
|
4 |
Beri |
Be |
9 |
II |
|
5 |
Bo |
B |
11 |
III |
|
6 |
Cacbon |
C |
12 |
IV, II |
|
7 |
Nitơ |
N |
14 |
II, III, IV… |
|
8 |
Oxi |
O |
16 |
II |
|
9 |
Flo |
F |
19 |
I |
|
10 |
Neon |
Ne |
20 |
|
|
11 |
Natri |
Na |
23 |
I |
|
12 |
Magie |
Mg |
24 |
II |
|
13 |
Nhôm |
Al |
27 |
III |
|
14 |
Silic |
Si |
28 |
IV |
|
15 |
Photpho |
P |
31 |
III, V |
|
16 |
Lưu huỳnh |
S |
32 |
II, IV, VI |
|
17 |
Clo |
Cl |
35,5 |
I,… |
|
18 |
Argon |
Ar |
39,9 |
|
|
19 |
Kali |
K |
39 |
I |
|
20 |
Canxi |
Ca |
40 |
II |
|
24 |
Crom |
Cr |
52 |
II, III |
|
25 |
Mangan |
Mn |
55 |
II, IV, VII… |
|
26 |
Sắt |
Fe |
56 |
II, III |
|
29 |
Đồng |
Cu |
64 |
I, II |
|
30 |
Kẽm |
Zn |
65 |
II |
|
35 |
Brom |
Br |
80 |
I… |
|
47 |
Bạc |
Ag |
108 |
I |
|
56 |
Bari |
Ba |
137 |
II |
|
80 |
Thuỷ ngân |
Hg |
201 |
I, II |
|
82 |
Chì |
Pb |
207 |
II, IV |
Chú thích:
- Chữ color đen: Nguyên tố kim loại
- Chữ color xanh: Nguyên tố phi kim
- Chữ color đỏ: Nguyên tố khí hiếm
Hóa trị của nhân tố là tổng số links chất hóa học tuy nhiên vẹn toàn tử của nhân tố cơ tạo thành nhập phân tử.
Bảng hóa trị tiếp tục bao hàm những vấn đề quan trọng như thương hiệu nhân tố, số proton, ký hiệu chất hóa học, vẹn toàn tử khối và hóa trị của nhân tố cơ. Thứ tự động của những nhân tố nhập bảng nhân tố chất hóa học sẽ được bố trí bám theo số proton tăng dần dần.
Tuy nhiên, những em nên ghi nhớ rằng, những nhân tố chất hóa học ko cần chỉ mất có một không hai một hóa trị. Cạnh cạnh một trong những nhân tố có một hóa trị như Hidro (I), Liti (I), Beri (II), Bo (III) thì đem những nhân tố đem 2 hóa trị như Cacbon (II, IV), Photpho (III, V), Crom (II, III) hoặc nhiều hơn nữa 2 như Nitơ (II, III, IV), Lưu huỳnh (II, IV, VI) hoặc Mangan (II, IV, VII),…
Có từng nào nhân tố hóa học?
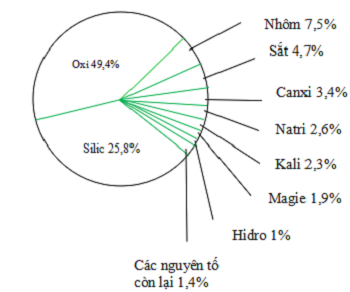
Hiện ni, những mái ấm khoa học tập vẫn tìm hiểu được tổng số 110 nhân tố hoá học tập. Trong số đó, 98 nhân tố chất hóa học đem xuất xứ kể từ ngẫu nhiên (trên Trái Đất, mặt mũi trời, mặt mũi trăng…), những nhân tố còn sót lại là tự tạo.
Bảng hóa trị một trong những group vẹn toàn tử
| STT | Tên gốc – group chức | Công thức chất hóa học group – gốc axit | Nguyên tử khối | Hóa Trị |
| 1 | Hidroxit | OH | 17 | I |
| 2 | Clorua | Cl | 35,5 | I |
| 3 | Nitrat | NO3 | 62 | I |
| 4 | Sunfat | SO4 | 96 | II |
| 5 | Cacbonat | CO3 | 60 | II |
| 6 | Clorat | ClO3 | 83.5 | I |
| 7 | Perclorat | ClO4 | 99.5 | I |
| 8 | ĐiHidro Photphat | H2PO4 | 98 | I |
| 9 | Hidro Photphat | HPO4 | 97 | II |
| 10 | Photphat | PO4 | 96 | III |
Để giải những bài bác tập luyện chất hóa học, cầm Chắn chắn bảng nhân tố hóa học cơ bạn dạng và hóa trị thôi ko đầy đủ, những em rất cần được ghi ghi nhớ tăng hóa trị của một trong những group vẹn toàn tử thông thường gặp gỡ như:
- Nhóm OH, NO3, Cl đem hóa trị I.
- Nhóm SO4, CO3 đem hóa trị II.
- Đặc biệt, những em cần thiết Note group đem số nhiều hóa trị không giống nhau là group PO4 đem hóa trị I, II, III. PO4 là gốc axit của axit photphoric (H3PO4), axit này còn có tính lão hóa tầm tuy nhiên rất có thể tạo nên trở thành 2 loại muối hạt bám theo 3 công thức không giống nhau. Cụ thể:
- H3PO4 tạo thành 2 muối hạt axit bám theo 2 công thức M(H2PO4)x, M2(HPO4)x và M là 1 trong những sắt kẽm kim loại này cơ.
Ví dụ: M là Natri (hóa trị I) tớ đem 2 công thức muối hạt axit là NaH2PO4 và Na2HPO4
- H3PO4 tạo thành muối hạt dung hòa bám theo công thức M3(PO4)x với M là sắt kẽm kim loại và x là số hóa trị của M.
Mẹo ghi nhớ nhanh chóng hóa trị của những nhân tố chất hóa học với bài bác ca hóa trị
Ghi ghi nhớ bảng nhân tố chất hóa học và bài bác ca hóa trị ko hề khó khăn giống như những em vẫn suy nghĩ. Để canh ty những em dễ dàng ghi nhớ những nhân tố chất hóa học, số hóa trị và canh ty môn học tập hạn chế thô khăn, những thầy cô vẫn sáng sủa tác nên nhiều bài bác ca hóa trị không giống nhau. Tuy nhiên, nhằm rời lầm lẫn, những em nên làm học tập nằm trong một bài bác. Sau đó là một vài ba bài bác ca hóa trị tuy nhiên những em rất có thể tìm hiểu thêm.
Bài ca hóa trị số 1:
Kali, Iot, Hidro
Natri với Bạc Bẽo, Clo một loài
Có hóa trị I các bạn ơi
Nhớ ghi mang lại rõ ràng kẻo rồi phân vân
Magie, Chì, Kẽm, Thủy ngân
Canxi, Đồng ấy cũng xấp xỉ Bari
Cuối nằm trong tăng chú Oxi
Hóa trị II ấy đem gì khó khăn khăn
Bác Nhôm hóa trị III lần
Ghi sâu sắc trí ghi nhớ Lúc cần phải có ngay
Cacbon, Silic này đây
Là hóa trị IV ko thời nay quên
Sắt cơ kể cũng thân quen tên
II, III tăng giảm thiệt phiền lắm thay
Nitơ phiền nhiễu nhất đời
I, II, III, IV Lúc thìa là V
Lưu huỳnh lắm khi nghịch ngợm khăm
Lúc II, khi VI Lúc ở loại IV
Photpho thưa cho tới ko dư
Nếu ai chất vấn cho tới thì ừ rằng V
Bạn ơi nỗ lực học tập chăm
Bài ca hóa trị xuyên suốt năm rất rất cần
Bài ca hóa trị số 2:
Hidro (H) cùng theo với liti (Li)
Natri (Na) cùng theo với kali (K) chẳng rời
Ngoài đi ra còn bạc (Ag) sáng sủa ngời
Chỉ đem hóa trị I thôi chớ nhầm
Riêng đồng (Cu) cùng theo với thuỷ ngân (Hg)
Thường II không nhiều I chớ lăn tăn gì
Đổi thay cho II, IV là chì (Pb)
Điển hình hoá trị của chì là II
Bao giờ nằm trong hoá trị II
Là oxi (O), kẽm(Zn) chẳng sai chút gì
Ngoài đi ra còn tồn tại can xi (Ca)
Magiê (Mg) cùng theo với bari (Ba) một nhà
Bo (B), nhôm (Al) thì hóa trị III
Cacbon, Silic (Si), thiếc (Sn) là IV thôi
Thế tuy nhiên cần thưa tăng lời
Hóa trị II vẫn chính là điểm cút về
Sắt (Fe) II toan tính bộn bề
Không bền nên dễ dàng trở thành ngay tắp lự Fe III
Photpho III không nhiều gặp gỡ mà
Photpho V chủ yếu người tớ gặp gỡ nhiều
Nitơ (N) hoá trị bao nhiêu?
I, II, III, IV phần nhiều cho tới V
Lưu huỳnh lắm khi nghịch ngợm khăm
Khi II khi IV, VI tăng tột cùng
Clo Iot lung tung
II III V VII thông thường thì I thôi
Mangan phiền nhiễu nhất đời
Đổi kể từ I cho tới VII thời mới nhất yên
Hoá trị II người sử dụng rất rất nhiều
Hoá trị VII cũng khá được yêu thương hoặc cần
Bài ca hoá trị nằm trong lòng
Viết thông công thức dự phòng lãng quên
Học hành nỗ lực cần thiết chuyên
Siêng ôn siêng luyện tất yếu ghi nhớ nhiều

Bài tập luyện về xác lập hóa trị của những nhân tố hóa học
Bài tập luyện 1: Xác ấn định hóa trị của những vẹn toàn tố
a. Al nhập hợp ý hóa học Al2O3
b. Fe nhập hợp ý hóa học FeO
c. Cr nhập hợp ý hóa học CrO và Cr2O3
Phương pháp giải:
- Gọi a là hóa trị cần thiết xác lập của nhân tố nhập hợp ý chất
- Xác ấn định hóa trị của nhân tố còn lại
- Áp dụng quy tắc hóa trị
Lời giải:
a.
Gọi a là hóa trị cần thiết xác lập của Al nhập hợp ý hóa học Al2O3
Trong hợp ý hóa học Al2O3, O đem hóa trị II.
Áp dụng quy tắc hóa trị tớ có: a.2 = 2.3
⇔ a = 3 (III)
Vậy hóa trị của Al nhập hợp ý hóa học Al2O3 là III.
Tương tự
b. Hóa trị của Fe nhập hợp ý hóa học FeO là II.
c.
Hóa trị của Cr nhập hợp ý hóa học CrO là II.
Hóa trị của Cr nhập hợp ý hóa học Cr2O3 là III.
Bài tập luyện 2: Cho 7 hợp ý hóa học với công thức chất hóa học như sau MgCl, NaO, BaO, NaCl, AlO3, K2O, Fe2O3. Dựa nhập bảng hóa trị những nhân tố cho biết thêm những công thức này ghi chép đích thị và ghi chép sai.
Phương pháp giải:
- Xác ấn định chỉ số và hóa trị của những nhân tố nhập hợp ý chất
- Áp dụng quy tắc hóa trị
- Nếu đẳng thức bám theo quy tắc hóa trị đích thị thì công thức ghi chép đích thị và ngược lại
Lời giải:
Các công thức chất hóa học ghi chép đích thị bao gồm BaO, K2O, Fe2O3.
Các công thức chất hóa học bao gồm MgCl (MgCl2); NaO (Na2O); AlO3 (Al2O3).
Bài tập luyện 3: Lập công thức chất hóa học của những hợp ý hóa học bên dưới đây:
a. C (IV) và S (II)
b. Fe (II) và O
c. N (V) và O
Phương pháp giải:
\begin{aligned}
& \small \text{Bước 1: Viết công thức chất hóa học công cộng của hợp ý chất: } M_xN_y
\\
& \small \text{Bước 2: Xác ấn định m và n theo lần lượt là hóa trị của 2 nhân tố M và n.}
\\
& \small \text{Bước 3: Xây dựng đẳng thức bám theo quy tắc hóa trị: } m.x = n.y
\\
& \small \text{Bước 4: Chuyển đẳng thức bên trên về dạng phân thức: } \frac{x}{y} = \frac{n}{m} = \frac{n'}{m'}
\\
& \small \text{Bước 5: Chọn x = m' và nó = n' với m' và n' vẹn toàn dương sao mang lại phân thức } \frac{m'}{n'} \text{ tối giản}
\end{aligned}
Lời giải:
\begin{aligned}
& \small \text{a.}
\\
& \small \text{Gọi x và nó theo lần lượt là chỉ số của 2 nhân tố C và S, công thức chất hóa học công cộng của hợp ý hóa học là } C_xS_y
\\
& \small \text{Hóa trị của 2 nhân tố C và là theo lần lượt là IV và II.}
\\
& \small \text{Theo quy tắc hóa trị, tớ có: } 4.x = 2.y
\\
& \small \iff \frac{x}{y} = \frac{2}{4} = \frac{1}{2}
\\
& \small \text{Chọn x = 1 và nó = 2, công thức chất hóa học của hợp ý hóa học là } CS_2.
\end{aligned}
Tương tự
b. Công thức chất hóa học của hợp ý hóa học là Fe2O3.
c. Công thức chất hóa học của hợp ý hóa học là P2O5.
Xem thêm: Bí quyết đổi tên Facebook chỉ 1 chữ năm 2023, đặt tên FB 1 chữ trên Android và iPhone
Tham khảo tức thì những khoá học tập online của Marathon Education
Team Marathon một vừa hai phải share cho những em những kỹ năng về bảng nhân tố hóa học và bài bác ca hóa trị. Học hóa cũng khá thú vị cần ko nào? Hy vọng, những vấn đề hữu ích nhập nội dung bài viết này sẽ hỗ trợ mang lại việc học tập của những em trở thành nhẹ dịu, không nhiều áp lực nặng nề rộng lớn.
Hãy tương tác tức thì với Marathon và để được tư vấn nếu như những em mong muốn học online nâng lên kỹ năng nhé! Marathon Education chúc những em được điểm trên cao trong số bài bác đánh giá và kỳ thi đua chuẩn bị tới!











Bình luận